近日,金迪安®淋球菌、沙眼衣原体、解脲脲原体核酸检测试剂盒(荧光PCR法)一管检三型核酸检测试剂盒,获得国家药品监督管理局颁发的三类产品注册证(注册证号:国械注准20203400150),这个产品的获批标志金迪安感染类分子诊断检测试剂形成系列,在性传播疾病诊断方面提供了一个新的产品,同时实现CT、NG、UU一管检三型的技术创新,为后续产品推广上市奠定了基础。

这个产品是金迪安®分子诊断平台继新型冠状病毒(2019-nCoV)核酸检测试剂盒(荧光PCR法)研发成功并完成注册检验、申报国家药品监督管理局之后的又一新产品获批。
性传播疾病(STD)是一组主要由性接触或类似性行为接触为主要传播途径的严重危害人群身心健康的传染性疾病。NG、CT、UU为STD重要感染病原体。据世界卫生组织(WHO)2016年统计,全球每年有1.27亿成年人感染CT,8700万患淋病,每天约有100万人感染STD。
本产品主要用于定性检测男性尿道拭子样本、女性宫颈拭子样本等中的淋球菌(NG)、沙眼衣原体(CT)、解脲脲原体(UU)DNA。检测结果可用于NG、CT、UU感染的辅助诊断,为性病的早期诊断以及性病高危人群的初筛提供分子诊断依据。
产品特点:
检测平台:多重荧光PCR技术,一管检三型;
检测通量:96测试/次,2小时完成;
检 测 限:CT≤500 copies/mL、NG/UU≤1000 copies/mL;
自 动 化:磁珠核酸提取+PCR扩增检测,可实现自动化;
内标质控:全程质控提取、检测过程,避免假阴性;
特 异 性:特异性探针设计,与其他病原体无交叉污染;
防 污 染:dUTP+UNG酶有效防产物污染。
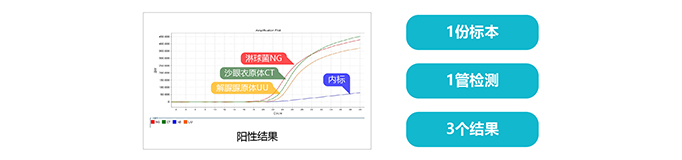
产品应用:
CT-NG-UU与性传播疾病筛查:
CT、NG、UU多数处于无症状感染,成年女性淋球菌(NG)78%无症状,沙眼衣原(CT) 70%无自觉症状,出现合并症状才会被发现,主要通过性行为传播,引起生殖系统、泌尿系统传播疾病;
CT-NG-UU与生殖道感染筛查:
CT/NG 感染对女性生殖健康造成深远影响,可导致阴道炎、宫颈炎、盆腔炎,甚至是不孕症、早产流产等;CT/UU混合感染增加女性不孕不育的感染风险;
CT-NG-UU与泌尿系统感染筛查:
淋病性尿道炎主要是NG感染,非淋病性尿道炎主要是CT(25- 50%)、UU(20-40%)合并感染,生殖支原体(12-20%)等。
随着本产品的获批上市,目前金迪安分子诊断平台已经完成了系统平台建设,实现了自主研发仪器设备+试剂耗材的整体解决方案。检测设备:金迪安MC-1000荧光定量PCR仪和金迪安EB-1000自动核酸提取仪,诊断试剂:(HPV)23分型检测试剂盒、HBV定量检测试剂盒、2019-nCoV 检测试剂盒、CT/NG/UU一管检三型试剂盒。



